纳米刺客出击:中科院首创肿瘤细胞自毁新策略
7月18日消息,人类免疫系统中的CD8T细胞原本是清除异常细胞的“杀手锏”,但在面对实体肿瘤时却常常“失灵”。这一现象揭示了当前癌症治疗中一个亟待突破的难题。尽管医学研究不断取得进展,但如何激活或恢复这些免疫细胞的功能,仍是科学家们关注的核心问题之一。这一发现不仅为未来治疗策略提供了新方向,也提醒我们,在对抗癌症的道路上,仍需持续探索与创新。
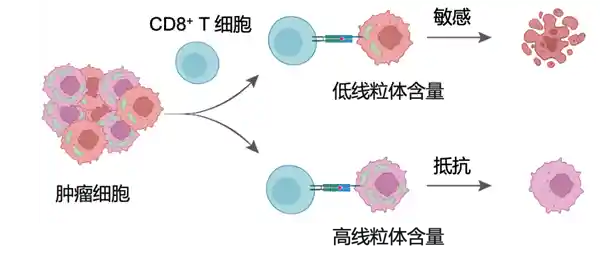
关键原因在于肿瘤细胞的线粒体——这些“能量工厂”不仅支撑肿瘤代谢,还通过抑制免疫信号、争夺营养等方式构建免疫抑制微环境,从而削弱免疫系统的攻击能力。线粒体越丰富的肿瘤细胞,其抵抗能力往往越强。 从医学研究的角度来看,这一发现为未来抗肿瘤治疗提供了新的方向。如果能够有效干预线粒体的功能或数量,或许可以打破肿瘤细胞的防御机制,提升免疫疗法的效果。这不仅是对肿瘤生物学理解的深化,也为临床治疗带来了更多可能性。
CD8+T更倾向于杀伤线粒体含量较低的肿瘤细胞
中国科学院国家纳米科学中心的研究团队研制出一种名为mitoNIDs的纳米降解剂,为应对这一问题提供了新的解决方案。
其核心是“纳米诱导临近技术”:如同“牵线搭桥”,让原本距离较远的生物分子靠近以触发特定反应。
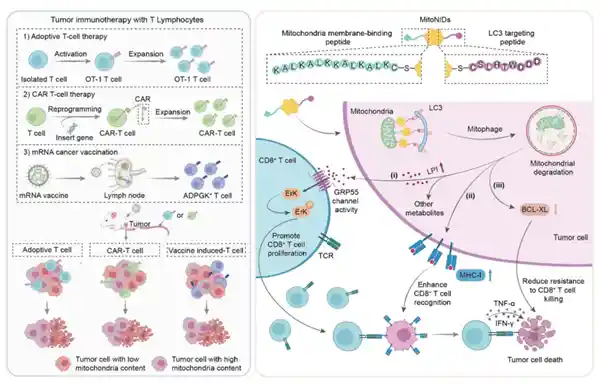
mitoNIDs是一种由金纳米颗粒构成的双功能系统,其一端利用线粒体靶向肽将药物精准引导至癌细胞的线粒体区域,另一端则连接自噬相关蛋白LC3的识别肽,促使线粒体与自噬机制相互靠近,从而触发选择性自噬过程,实现对线粒体的降解。 这一技术在癌症治疗领域展现出新的可能性。通过精准调控线粒体与自噬系统的相互作用,不仅提高了治疗的靶向性,也增强了对癌细胞的杀伤效果。这种结合纳米技术和生物分子的创新方式,为未来开发更高效、更安全的抗癌疗法提供了重要参考。
纳米诱导临近剂精准诱导肿瘤细胞“自毁线粒体”以增强免疫治疗效果。这一技术通过利用纳米材料,精准作用于肿瘤细胞的线粒体,触发其自我破坏机制,从而提升免疫系统对肿瘤的识别与杀伤能力。该方法在实验中展现出良好的安全性和有效性,为未来肿瘤治疗提供了新的思路和可能。 这种技术的出现,标志着癌症治疗正逐步从传统的“杀伤”模式向更精准、更智能的方向发展。通过干预肿瘤细胞的关键代谢环节,不仅提高了治疗的针对性,也减少了对正常组织的损伤。随着研究的深入,此类创新手段有望在临床中得到广泛应用,为患者带来更优的治疗方案。
线粒体被降解后,CD8+T细胞战斗力从三方面提升:肿瘤细胞表面MHC-I分子增多,更易被识别;抗凋亡蛋白BCL-XL减少,癌细胞更易被击杀;线粒体降解释放的信号分子溶血磷脂酰肌醇,能激活T细胞活性。
在小动物肿瘤模型中,mitoNIDs与免疫疗法联合使用已展现出显著的肿瘤抑制效果,这一成果为未来癌症治疗提供了新的方向,后续仍需通过临床试验进一步验证其安全性和有效性。 我认为,这一研究进展表明,结合线粒体靶向治疗与免疫手段可能成为抗肿瘤策略的重要突破。尽管目前仍处于动物实验阶段,但其潜在价值不容忽视。未来若能在临床中取得类似效果,将为患者带来更有效的治疗选择。同时,也提醒我们,从基础研究到临床应用之间仍需克服诸多挑战,科学探索的脚步不能停歇。
未来,这类纳米“牵线搭桥”技术有望拓展至自身免疫病、神经退行性疾病等多个领域,助力人类在分子层面实现对生命过程的精准调控。
免责声明:本站所有文章来源于网络或投稿,如果任何问题,请联系648751016@qq.com
页面执行时间0.009822秒